Аминокислотами называются органические кислоты, содержащие одну или несколько аминогрупп.
В зависимости от положения аминогруппы по отношению к карбоксилу различают α, β и γ-аминокислоты:
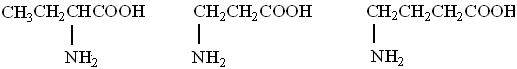
α-аминомаслянаяβ-аминопропионоваяγ-аминомасляная
Все α- аминокислоты, кроме аминоуксусной (глицина), имеют асимметрический α-углеродный атом и существуют в виде двух энантиомеров. За редким исключением, природные а -аминокислоты относятся к L- ряду (S-конфигурация) и имеют следующее пространственное строение
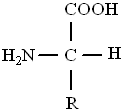
||По физическим и ряду химических свойств аминокислоты резко отличаются от соответствующих кислот и оснований. Они лучше растворяются в воде, чем в органических растворителях; хорошо кристаллизуются; имеют высокую плотность и исключительно высокие температуры плавления. Эти свойства указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твёрдом состоянии и в растворе (в широком интервале рН) находятся в цвиттер-ионной форме (т.е. как внутренние соли). Взаимное влияние групп особенно ярко проявляется у α- аминокислот, где обе группы находятся в непосредственной близости.
Цвиттер-ионная структура аминокислот подтверждается их большим дипольным моментом, а также полосой поглощения в ИК- спектре твердой аминокислоты или её раствора.
Все аминокислоты отличаются характером радикала, который может быть ациклическим или циклическим. В состав радикала может входить дополнительно вторая карбоксильная группа (такие аминокислоты называются моноаминодикарбоновые МАДК) или две аминные группы (диаминомонокарбоновые ДАМК). В составе отдельных аминокислот могут находиться гидроксильные группы (серин, треонин),сульфгидрильная (цистеин), метильная (метионин).
Таблица 1. Важнейшие аминокислоты.
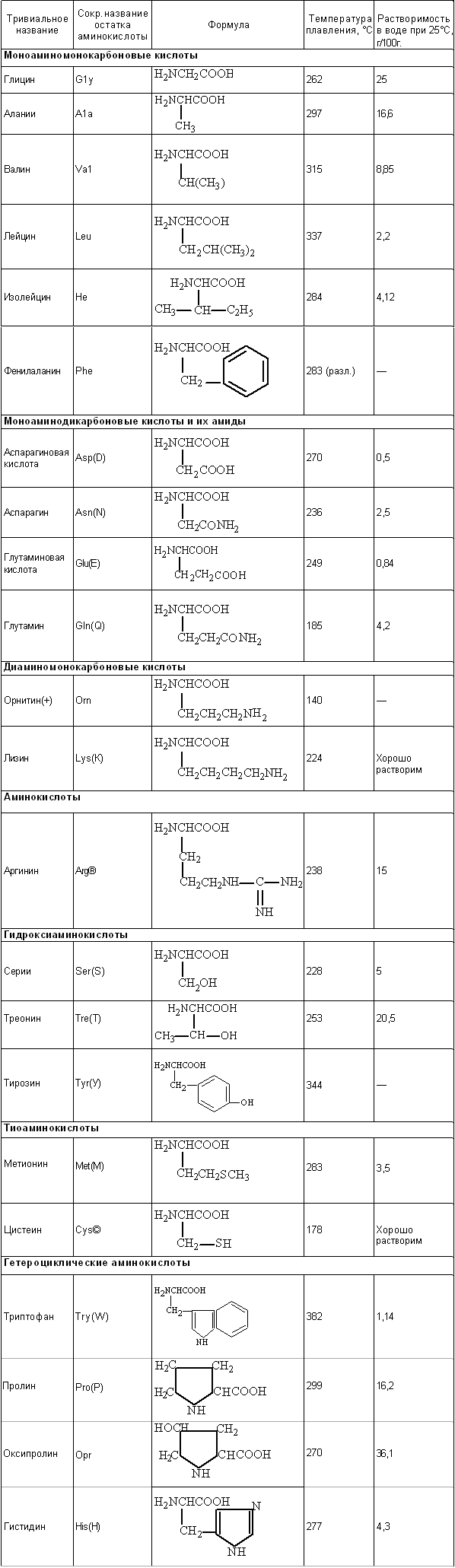
Большинство аминокислот, участвующих в обменных процессах и входящих в состав белков, могут поступать с пищей или синтезироваться в организме в процессе обмена ( из других аминокислот, поступающих в избытке). Они называются заменимыми. Некоторые аминокислоты не могут синтезироваться в организме и должны поступать с пищей - незаменимые аминокислоты. Таких аминокислот девять (гистидин, триптофан, фенилаланин, лизин, метионин, треонин, изолейцин, лейцин, валин).